作者:马兴元 摄影:马兴元
近日,美国化学会(The American Chemical Society)旗下的合成生学(ACS Synthetic Biology)杂志以“Enhanced biosynthesis performance of heterologous proteins in CHO-K1 cells using CRISPR-Cas9”(DOI: 10.1021/acssynbio.7b00375)为题,在线报道了beat365官网生物反应器工程国家重点实验室马兴元教授的生物药学团队,在哺乳动物细胞基因组编辑与抗体合成生物学研究领域所取得的重要进展。beat365官网为该论文的第一作者单位,beat365官网2014级硕士研究生王文鹏和郑文云副教授为该论文的第一作者。课题研究同时也得到了来自美国北卡罗来大学A/Prof. Wenliang Zhang和厦门大学刘海鹏教授的大力支持,同为论文的通讯作者。
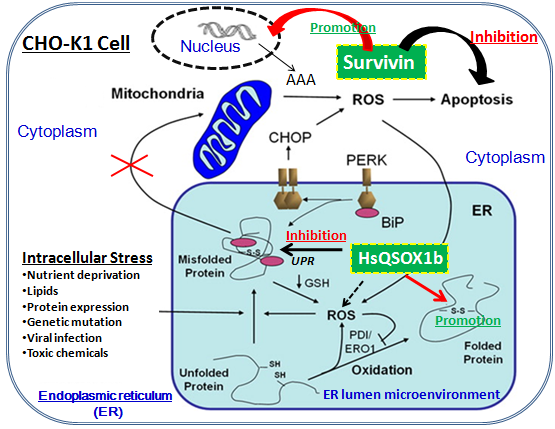
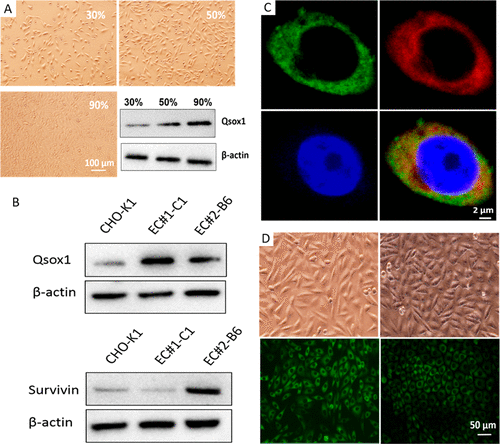
生物技术药物已经成为我国医药产业的支柱产业和朝阳产业,特别是基因工程疫苗和抗体产业,为人民身体健康提供了重要保障。哺乳动物细胞表达系统在基因工程抗体和疫苗中具有举足轻重的地位,特别是中国仓鼠卵巢细胞(Chinese Hamster Ovary,CHO),是目前治疗性抗体生产的首选宿主,约70%的抗体蛋白是由CHO细胞生产的。然而尽管CHO细胞最早来源于我国的仓鼠,但是目前生产抗体的优质细胞株,却基本掌控在国外大制药公司,作为核心技术而无法购得,这严重制约着我国抗体产业的质量提升和经济成本。另外,抗体类药物临床使用剂量大和动物细胞表达抗体效能普遍较低的矛盾也制约抗体药物的生产成本和临床价格。因此,如何从根本上提高动物细胞生产抗体的性能一直是业界关注的热点.
本研究基于细胞合成生物学理论,利用CRISPR/Cas9基因编辑先进技术,对常规市售CHO-K1细胞开展了人源HsQSOX1b和Survivin的双基因精准编辑,在建立快速高效的宿主细胞改造技术平台的同时,并以eGFP和GLuc2种蛋白为示范,在探究内质网中二硫键形成与蛋白质折叠、内质网未折叠蛋白应激反应(UPR)和细胞抗凋亡三者之间的分子机制基础上,成功地获得了比未经编辑的对照细胞株抗凋亡能力提升6.4倍、目的模式蛋白产量提高5.5倍的双基因编辑细胞株(CHO-K1-EC2) , 这将为我国从源头强化抗体高效生产细胞株提供了重要的理论依据,同时有望为我国广大民众未来用得起价廉、安全、高效的生物技术药物提供重要的技术支撑。
马兴元教授一直致力于针对癌症和传染病防治的新型抗体和疫苗生物药物和新型载药制剂研发,并与国内外相关学者和企业广泛开展了较有成效的产学研合作,且取得了一系列较好成果和成效。特别是在载药生物材料领域,与校外合作共同研究,近来也取得了新成果,刚被美国化学会生物材料工程(ACS Biomater. Sci. Eng)(DOI: 10.1021/acsbiomaterials.8b00260)杂志在线发表,这将为抗癌新药研发奠定了重要基础。
相关项目也得到了国家“新药创制”重大专项、国家自然科学基金和上海科技创新“行动计划”等项目的资助。
论文链接:
ACSSynth. Biol.:https://pubs.acs.org/doi/full/10.1021/acssynbio.7b00375
ACS Biomater. Sci. Eng.:https://pubs.acs.org/doi/full/10.1021/acsbiomaterials.8b00260